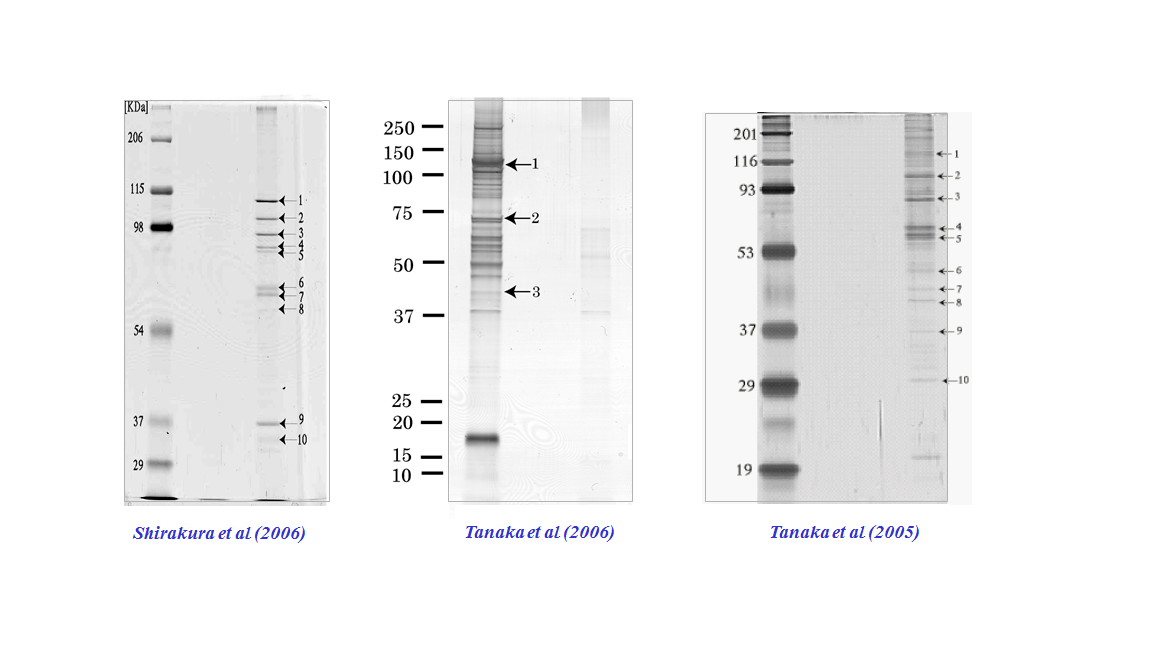
2. タンパク質凝集体の形成メカニズムの解明
細胞内のタンパク質の存在量は、タンパク質の合成と分解のバランスによって調節されています。しかしながら、何らかの原因でこのバランスが崩れると、(ある種の)タンパク質は凝集し、不溶性の構造物となって細胞内に沈着します。アルツハイマー病やパーキンソン病などの神経変性疾患では、異常タンパク質からなる凝集体の沈着が実際に観察されています。こうした凝集体が形成されるメカニズムはまだほとんど分かっていません。
わたしたちは他大学と共同で、正常・異常タンパク質からなる凝集体形成の分子機構解明を目指した研究を行っています。これまでの研究で、TRIM32というタンパク質がつくる凝集体の形成に、一群の分子シャペロンタンパク質が関与していることを明らかにしています。今後は、上述したプロテオミクスの解析技術を適用することで、これまでの研究をさらに発展させるとともに、多くの疾患関連凝集体の形成に共通する分子機構の解明に迫りたいと考えています。
|

|
3. ミトコンドリアの融合/分裂を支配する新しい分子装置の解明
ミトコンドリアは融合と分裂を繰り返し行っている重要なオルガネラです。ミトコンドリアの構造変化は、細胞生存にとって必須であり、その異常はさまざまな病気と関係します。しかしながら、高等動物ミトコンドリアの構造変化の研究は,酵母やショウジョウバエを用いて得られた遺伝学的解析データをそのまま動物細胞に適用したものがほとんどです。全容解明には未だ至っていない状況です。
わたしたちは他大学との共同研究を通して、ミトコンドリアの融合/分裂を支配する新しい高等動物細胞分子装置の同定を目指した研究を進めています。この目的のために、上述したタンパク質間相互作用解析を高等動物ミトコンドリアタンパク質にフォーカスさせて研究を展開しています。
|
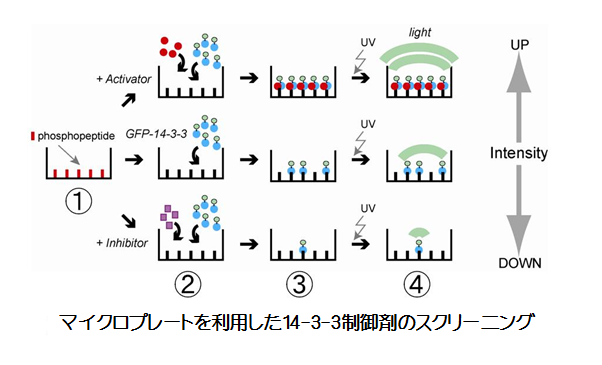
4. 14-3-3タンパク質のリン酸化依存性相互作用をターゲットとする創薬シーズの開発
14-3-3は、キナーゼによるリン酸化反応に依存して多種多様なタンパク質と複合体を形成します。さらに、これらの標的にはガンや神経変性疾患などの難治性疾患と関係する分子が非常にたくさん含まれていす。そこで、14-3-3のリン酸化依存性相互作用を選択的に制御できる低分子化合物を、公的・民間企業から提供される化合物ライブラリーの大規模スクリーニングによって発掘しようと考えています。14-3-3の選択的制御剤が開発されることは、同分野ならびに関連する医薬学系の基礎・応用分野において、生命現象や病気機構の解明が飛躍的に進むことが期待できるからです。
|
|